人医学系研究開始までの流れ
人医学系研究等を実施する際は、適切な倫理審査申請手続きを行い、倫理審査委員会及び研究機関の長の「承認」を得る必要があります。
注意!
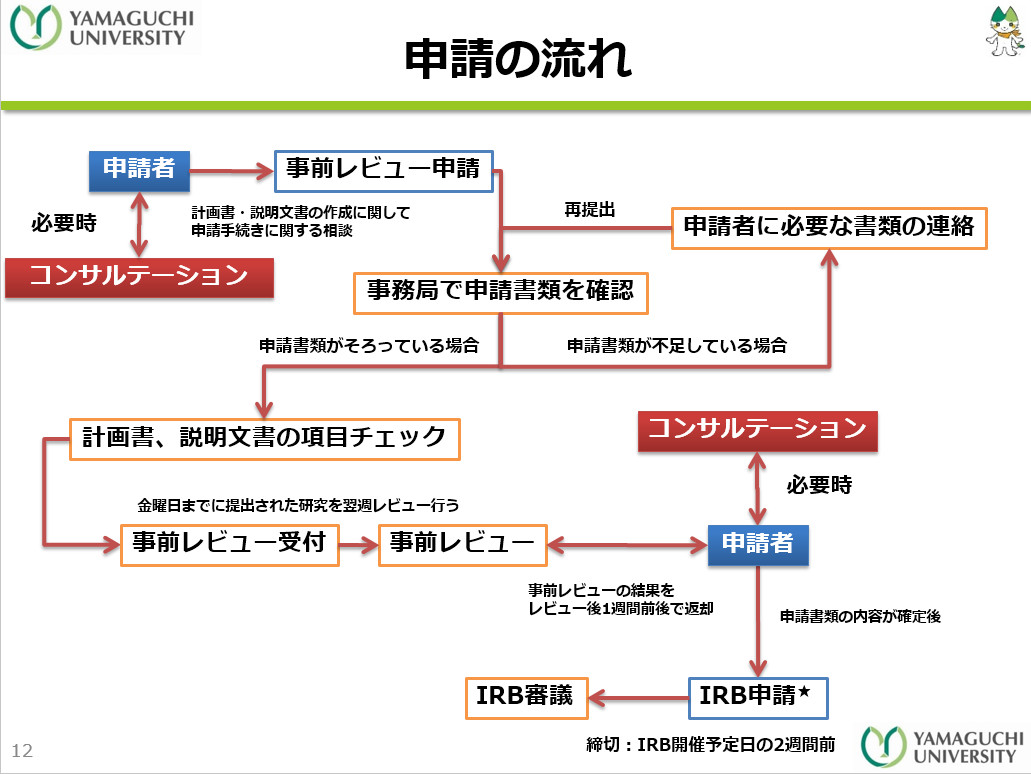
倫理審査申請手続きにはいくつかの段階があります。②事前レビューから④倫理審査までに早くとも2ヶ月程度の時間を要します。余裕をもって、ご準備ください。
研究開始までの流れは以下の通りです。

-
事前準備(コンサルテーション・書類作成等)
倫理審査に必要な申請書類は、実施する研究デザインによって異なります。
まずは自分が実施したい研究がどの研究デザインに該当するのかを確認してください。
※「人医学系研究等を実施するみなさんへ」P.5 デジションツリー
研究デザインを確認したら、デザインごとに必要な書類の作成してください。
臨床研究センターでは、計画書や同意説明文書等の必要書類の雛形を提供しています。
ご活用ください。
※計画書等ひな形のダウンロードページはこちら(人医学系研究手続き)
倫理審査申請には計画書や同意説明文書のほかに、申請書式が必要です。
申請書式の作成は「臨床試験申請支援システム」を利用してください。
多施設共同研究に参画する場合は「人医学系研究等を実施するみなさんへ」P.11を確認し必要書類の準備をお願いします。(確認事項回答書はセンターから連絡しますので、初回申請時は不要です。)
山口大学倫理審査委員会に審査依頼を行う場合には、臨床研究支援システムを利用した手続きが必須となります。 ただし、本システムはWidnowsのみしか対応できていないため、Macintoshをご利用の研究者は別途ご相談ください。 -
事前レビュー
倫理審査に必要な申請書類を作成したら、「臨床試験申請支援システム」から出力した申請データをメールに添付して、臨床研究センター宛(clin_res@yamaguchi-u.ac.jp)に送付してください。 明らかに必要な書類が不足していたり、雛形の不適合等の不備がある場合は、事前レビューが受け付けられません。修正依頼のメールが返送されますので、ご対応ください。 事前レビューの結果はメールにて返却され、確認事項や指摘事項についてセンタースタッフとのやり取りが開始します。必要書類が完成するまで数回のやり取りを行います。事前レビューとはIRBでの本審査前に、指針に定められた必要事項の記載が充足しているか、記載内容・提出書類に不備や不足がないかの確認を行います。 金曜日までに受け付けたものは、翌水曜日に事前レビューを行い、そこから10日前後で結果が返却されます。 -
捺印済み書類提出
必要書類が完成したら、臨床研究センターからメールにて捺印済み書類提出依頼をします。 全ての申請書類を片面カラーで印刷し、ご捺印の上、ご提出ください。 書類の提出期限は毎月第2水曜日(IRB2週間前)です。IRB開催日や祝日に伴い変動することがありますので、日程等詳細はトップページよりご確認ください。 -
倫理審査
IRBは、基本的に毎月第4水曜日に開催されます。日程等詳細はトップページよりご確認ください。
審査結果はIRB終了後1週間前後でメール及び書面にて返却します。
早く結果が知りたい場合は、IRB翌日以降にお電話にてお問い合わせください。
-
研究開始
倫理審査委員会にて「承認」されると、いよいよ研究開始です。 研究を開始した後も、変更申請・有害事象報告・実施状況報告等、引き続き、適切な倫理審査手続きが必要です。 何か困ったことやご不明な点があれば、すぐに臨床研究センターにお問合せください。